IL MODELLO “A CATENA” DELLA SALUTE UMANA BASATO SULLA SCIENZA DEI TELOMERI

ABSTRACT
L'“effetto imbuto” dei telomeri descrive la convergenza, parziale indipendenza ed equivalenza dei nove principali fattori (nutrizionali, motori, psicologici, ecc.) sui telomeri, le strutture cromosomiche che rappresentano il nostro orologio biologico perché determinano la nostra longevità e la nostra qualità di vita globale.
L'“effetto imbuto” ha come logica conseguenza uno specifico modello bio-psico-sociale caratterizzato dall’equipollenza dei nove principali fattori (genetici ed epigenetici) nell’influenzare la nostra salute ed il nostro benessere.
Lo specifico modello a “catena”, che deriva da questo "effetto imbuto” dei telomeri, descrive proprio la parziale indipendenza ed equivalenza dei nove principali fattori che agiscono nel nostro organismo.
Le caratteristiche del modello a “catena” della salute e del benessere umano prevede alcune dinamiche quali, ad esempio, il fatto che “la catena è forte quanto il più debole dei suoi anelli” quindi è sufficiente la scarsità di un solo fattore (nutrizionale, motorio, psicologico, ecc.) per accelerare l’invecchiamento del nostro organismo con conseguente riduzione della longevità e l’aumento delle probabilità di sviluppare una serie di malattie.
Questo modello a-gerarchico, fortemente interconnesso ed integrato di benessere e salute umana ha implicazioni cliniche molto rilevanti in parte contrastanti alcuni assunti largamente condivisi anche all’interno della comunità di professionisti della salute.
Il presente scritto descrive alcune di queste implicazioni molto impattanti sulle effettive strategie previste da questo originale modello per migliorare il nostro benessere e la nostra salute umana.
--
Ormai la letteratura scientifica ha chiaramente identificato il ruolo fondamentale dei telomeri nel proteggere i cromosomi garantendo la loro stabilità genetica ed influenzando la salute ed il benessere umano (Armanios, & Blackburn, 2012; Aubert & Lansdorp, 2008; Blackburn, Epel, & Lin, 2015; Cawthon, et al., 2003; Fitzpatrick, et al., 2007; Valdes et al., 2005).
Queste strutture biologiche situate alle estremità di ciascun cromosoma sono composte, nella specie umana, da ripetizioni di sequenze di basi azotate non codificanti (5'-TTAGGG-3') che garantiscono la solidità strutturale del resto del cromosoma.
Ad ogni replicazione cellulare i telomeri si accorciano arrivando ad un numero massimo di replicazioni (il cosiddetto limite di Hayflick), che corrisponde ad una determinata lunghezza dei telomeri stessi (e quindi un determinato numero di basi azotate), superato il quale non è più garantita una sufficiente capacità di mantenimento strutturale del cromosoma (Hayflick & Moorhead, 1961).
In altri termini, se inizialmente la cellula zigote dispone di una lunghezza dei telomeri di circa 20 mila coppe di basi di DNA, già nel momento del parto queste strutture sono composte da circa 15 mila basi azotate ma nel momento in cui questo quantitativo arriva a circa 5 mila basi succede che la struttura dei telomeri non è più sufficiente a garantire la struttura del cromosoma.
Spesso, per far capire la funzione e la struttura dei telomeri, si utilizza la metafora dei terminali di plastica dei lacci delle scarpe che, se integri ed in buono stato, garantiscono a tutto il laccio di essere propriamente utilizzato ma, se si deteriorano oltre un certo limite, avviene lo sfilacciamento progressivo del tessuto che costituisce il laccio stesso.
In questa metafora il laccio rappresenta i nostri cromosomi ed il loro sfilacciamento raffigura il progressivo processo di invecchiamento, l’instabilità strutturale del cromosoma con la predisposizione allo sviluppo di malattie e la conseguente morte cellulare.
La lunghezza dei telomeri è cruciale nel determinare la longevità cellulare e la salute globale di tutto l'organismo per questo motivo la lunghezza dei telomeri è attualmente considerata il nostro “orologio” biologico più attendibile.
La lunghezza dei telomeri è influenzata dall'attività dell’enzima telomerasi perché il ruolo di questa struttura biologica è quello di manutenere e ricostruire, aggiungendo base azotate, i telomeri contrastandone quindi il fisiologico accorciamento (Andrews & Cornell, 2014; Andrews & Cornell, 2017; Armanios, 2013; Blackburn, 1991; Blackburn, 2010).
Sappiamo ormai già da una solida letteratura scientifica che diversi fattori quali gli stili di vita sani condizionano significativamente l’attività della telomerasi, e quindi la lunghezza dei telomeri, influenzando la longevità, la salute e la predisposizione a malattie legate all'invecchiamento (Cherkas et al., 2008; D'Mello et al., 2015; Shalev et al., 2013; Puterman et al., 2010; Tucker, 2017; Valdes et al., 2005).
È interessante notare che se è vero che nasciamo con una determinata lunghezza telomerica e che essa si accorcia progressivamente durante l’arco di vita di una persona, è altrettanto vero che la velocità relativa il “consumo” dei telomeri è estremamente variabile e dipendente da vari fattori che condizionano l’attività della telomerasi.
Infatti, mentre alcuni fattori “accelerano” l’accorciamento dei telomeri perché limitano l’azione manutentiva dalla telomerasi (pensiamo al fumare, al dormire poche ore, la sedentarietà, al distress psicosociale cronico, l’alimentazione scorretta, etc.) altri fattori ne “rallentano” il consumo perché promuovono più efficacemente l’attività della telomerasi (la meditazione, una regolare attività motoria, una corretta nutrizione, una corretta qualità del sonno, etc.) (Cherkas et al., 2008; Epel et al., 2016; Jackowska et al., 2012; Valdes et al., 2005).
Questa particolare dinamica relativa l’azione di accelerazione e rallentamento nel consumo dei telomeri è stata chiamata dal dott. Andrew Bill (scopritore della telomerasi) “tiro alla fune” dei telomeri perché descrive l’azione contrapposta di differenti fattori che determinano la lunghezza dei telomeri (Andrews & Cornell, 2017).
La Figura 1 rappresenta i telomeri e la telomerasi.
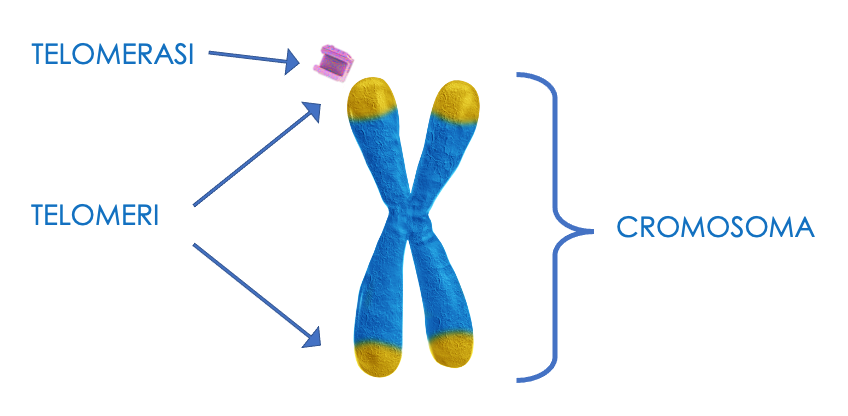
Figura 1: I telomeri e la telomerasi
In questa prospettiva potremmo dire che l’obiettivo terapeutico generale e relativo la prevenzione e la promozione della salute è quello di promuovere nel paziente il fisiologico accorciamento telomerico in maniera più lenta possibile favorendo la capacità manutentiva della telomerasi in modo da prolungare più possibile la longevità residua e di conseguenza la qualità di vita in termini anche di riduzione della probabilità di sviluppare problematiche cardiocircolatorie, immunitarie, etc. (Agnoletti, 2018a; Agnoletti, 2018b; Agnoletti, 2018c; Agnoletti, 2018d).
Abbiamo visto che la lunghezza iniziale dei telomeri è un parametro immodificabile comunque la velocità del suo consumo è fortemente influenzata dall’esposizione di fattori come il distress psicologico, gli inquinanti ambientali, l’abuso di fumo o di alcol e molti altri elementi che contribuiscono a definire il ritmo con il quale i nostri telomeri si accorciano determinando, in ultima analisi, la nostra longevità (Armanios & Blackburn, 2012; Blackburn, Epel & Lin, 2015; Calado & Young, 2009; López-Otín et al. 2013).
Analizzando la letteratura scientifica ho identificato nove fattori principali che determinano cambiamenti significativi nella lunghezza dei telomeri.
Questi nove fattori sono:
- la genetica;
- il benessere psicologico;
- l’alimentazione;
- il supporto sociale;
- i ritmi circadiani;
- l’ambiente fisico-chimico;
- il microbiota;
- il sonno;
- l’attività motoria.
La letteratura scientifica ha infatti evidenziato che il fattore genetico (Armanios & Blackburn, 2012; Calado & Young, 2009; Harley, Futcher & Greider, 1990; Liu & Khaing, 2012), il benessere psicologico (Epel et al., 2004; Epel et al., 2016; Gotlib & LeMoult, 2019; Price et al., 2013; Ridout et al., 2016; Zhang et al., 2016), il modo di alimentarci (Crous-Bou et al., 2014; Garcia-Calzon et al., 2014; Leung et al., 2018; Marcon et al.,2012; Niles & Terry, 2016), la qualità della rete sociale che percepiamo (Needham et al., 2015). O'Donovan et al., 2013; Puterman et al., 2013; Shalev et al., 2013; Steptoe et al., 2004), i ritmi circadiani (Carroll et al., 2016; Savolainen et al., 2014; Simon et al., 2006; Wen et al., 2015; Zhu et al., 2019), la qualità fisico-chimica dell’ambiente in cui viviamo (Blackburn & Epel, 2015; Clemente et al., 2020; Dioni et al., 2011; Hoxha et al., 2009; McGrath, Jones & Sorkin, 2017; Ward-Caviness et al., 2016), la composizione del microbiota che colonizza il nostro organismo (Ghosh et al. 2017; Liu et al. 2020; Jiang et al. 2017; Vaiserman & Krasnienkov, 2021), la qualità del sonno (Al-Hazzouri, et al., 2014; Carroll et al., 2016; Jackowska et al., 2012; Li & Wang, 2020; Prather et al., 2011) e l’attività motoria che facciamo (Cherkas et al., 2008; Lynch et al., 2020; Munstock et al., 2021; Puterman et al., 2010; Tejada-Garrido, Martín-Vallejo, & Navarro-López, 2024) contribuiscono tutti a determinare il ritmo di consumo dei telomeri e quindi dell’aspettativa di vita (in termini quantitativi e qualitativi).
Naturalmente tutti questi fattori, in parte, si influenzano vicendevolmente (pensiamo ad esempio a quanto l’attività motoria influenza la qualità del sonno o quanto i ritmi circadiani influenzano l’impatto metabolico dell’alimentazione) tuttavia ciascuno di questi fattori sono dotati anche di una certa autonomia per la loro complessa funzione e per il caratteristico meccanismo causale che influenza i telomeri.
Ad esempio, la gestione dello stress psicologico e la qualità ambientale fisico-chimica sono entrambi fattori che influenzano la lunghezza dei telomeri ma lo fanno in modo in parte indipendente l’uno dall’altro perché seguono percorsi causali almeno in parte differenti ed autonomi.
Ai fini di questo scritto risulta particolarmente interessante notare che attualmente la letteratura scientifica non evidenzia la dominanza di un fattore più importante rispetto gli altri ma descrive un effetto quantitativo dose dipendente per ciascuno di essi (Agnoletti, 2019; Blackburn, Epel & Lin, 2015; Bojesen, 2013; Epel et al., 2018; Lin, Epel, & Blackburn, 2012; Liu et al. 2018; Shammas, 2011; Starr et al., 2008; Valdes et al., 2005).
Come conseguenza di questa mancanza di dominanza di un fattore sugli altri (quello che potremmo chiamare “principio di equivalenza” dei fattori considerati), il fenomeno di accelerazione o rallentamento del consumo telomerico sembra essere, almeno in parte, indipendente dal tipo di meccanismo specifico che conduce ad alterare il funzionamento della telomerasi e quindi la lunghezza dei telomeri.
Di conseguenza il fenomeno di accelerazione o rallentamento dell’invecchiamento telomerico sembra essere almeno in parte indipendente dal tipo di percorso informazionale “a monte” che impatta sull’attività della telomerasi.
A tal proposito, ho coniato il termine “effetto imbuto” o “effetto collo di bottiglia” dei telomeri (Agnoletti, 2019) per descrivere la natura equivalente e convergente di tutti i nove macro-fattori identificati dalla letteratura scientifica (attività motoria, nutrizione, benessere psicologico, qualità del sonno, etc.) che, almeno in parte, indipendentemente influenzano la lunghezza dei telomeri.
La Figura 2 rappresenta l'"Effetto Imbuto" dei telomeri.
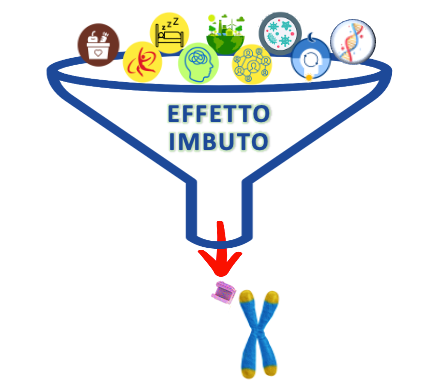
Fig 2: L'"Effetto Imbuto" dei telomeri
Le implicazioni dell’effetto imbuto sono molteplici e riguardano sia aspetti strettamente clinici che non (Agnoletti, 2021; Agnoletti, 2022).
Una delle più importanti implicazioni dell’“effetto imbuto” è che, nel contesto del paradigma bio-psico-sociale (Engels, 1977; Schwartz, 1982), esso definisce uno specifico modello di benessere e salute umana che può essere chiamato a “catena”.
Essendo che non vi è un fattore dominante sugli altri ma tutti i fattori contribuiscono in maniera equivalente ad influenzare la lunghezza dei telomeri (“principio di equivalenza”), il modello a “catena” prevede che la salute umana possa essere rappresentata da una catena composta da nove anelli dove ciascun anello della catena rappresenta uno specifico fattore.
Questo specifico modello, che riflette le evidenze descritte sopra derivanti dalla scienza dei telomeri, è coerente con l’approccio integrato previsto dal paradigma bio-psico-sociale, e presenta aspetti che contrastano parzialmente i modelli gerarchici e la cultura iper-specialistica relativi la salute e del benessere umano.
Nell’attuale periodo storico, i modelli gerarchici e la cultura iper-specialistica sono attualmente largamente condivisi anche all’interno delle comunità di professionisti del settore clinico (almeno nel mondo Occidentale).
Vediamo dunque alcune rilevanti implicazioni cliniche del modello bio-psico-sociale a “catena” del benessere e la salute umana.
Il modello a “catena” qui proposto implica che:
- sia necessaria inizialmente una valutazione globale dei nove fattori descritti;
- sia necessario dare priorità d’intervento al fattore, o ai fattori, più scarsi (perché rappresentano il fattore o i fattori, che rappresentano la maggiore vulnerabilità per i telomeri);
- l’obiettivo terapeutico generale non deve essere il raggiungimento «ottimale» in uno, o più fattori, ma l’evitamento della «scarsità» di uno, o più fattori.
Se la metafora della catena coglie la natura interconnessa e parzialmente indipendente dei nove principali fattori che influenzano la lunghezza dei telomeri, ne consegue che, per valutare lo stato globale della nostra salute risulta prioritario valutare contemporaneamente tutti e nove questi fattori al fine di identificare l’anello, o gli anelli, più deboli perché l’architettura logica di questo modello implica che “la catena è forte quanto il più debole dei suoi anelli”.
I professionisti del benessere e la salute umana dovrebbero avere come priorità iniziale la valutazione globale ed integrata prevista dal modello a “catena” appena descritto, al fine di identificare l’eventuale fattore, o gli eventuali fattori, che rappresentano per il paziente la maggiore vulnerabilità nei confronti dei telomeri.
Naturalmente questa priorità dovrebbe essere considerata a prescindere dall’ambito specialistico di ciascun professionista.
La Figura 3 rappresenta l'" Effetto Catena" della salute umana.
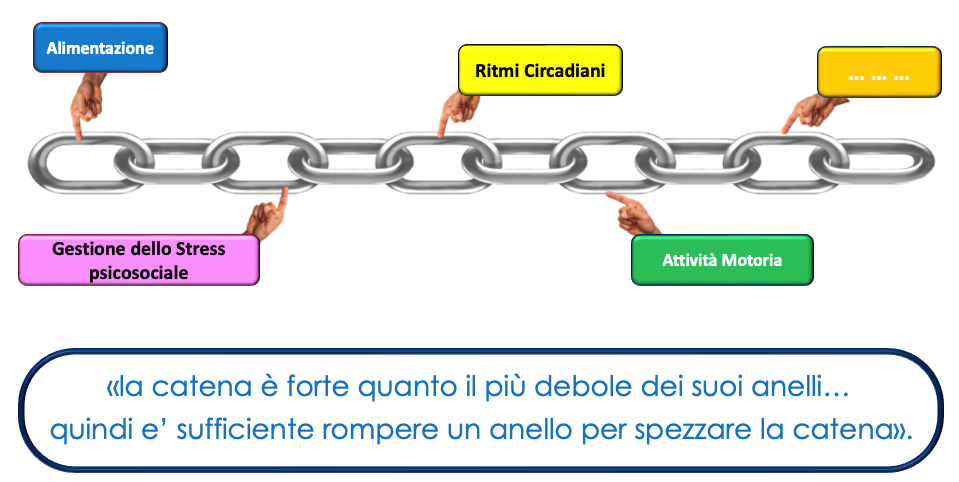
Figura 3: L'"Effetto Catena" della salute umana.
Se è vero, infatti, quanto descritto dall’ “effetto imbuto” e previsto dal modello a “catena” della salute umana, allora ha poco senso intervenire concentrandosi unicamente per esempio a livello psicologico, o esclusivamente sulla qualità del sonno, o motorio, o nutrizionale dal momento che l’impatto sui telomeri segue la logica descritta dal principio di “equivalenza” dei nove fattori.
Per il professionista, concentrarsi esclusivamente sul proprio specifico ambito d’intervento (per esempio quello psicologico o nutrizionale o motorio) senza tener conto della dinamica descritta dal modello a “catena”, rischia di essere poco efficace nel medio/lungo termine perché sottostimando uno o più “anelli” (per esempio quello relativo la qualità del sonno o dei ritmi circadiani) che richiederebbero invece un intervento più tempestivo, non si contrasta il fattore, o i fattori, che contribuiscono maggiormente ad accorciare i telomeri.
L’intervento dei professionisti dovrebbe invece tendere a “rinforzare” l’anello o gli anelli più deboli per raggiungere almeno un grado di sufficienza (pensiamo, ad esempio, ad un minimo di qualità del sonno o di attività motoria) ma non avere come obiettivo quello di “eccellere” in uno o più fattori a scapito di altri (si pensi ad esempio al caso in cui una persona aumenta significativamente la propria attività motoria ma contemporaneamente comincia ad alimentarsi scorrettamente).
Non effettuare un’iniziale analisi globale dei principali nove fattori previsti dal modello a “catena” ma continuare ad applicare una miope visione iper-specialistica della salute e del benessere umano implica dunque anche un potenziale rischio rappresentato dal fatto che il tempo e le energie investite in un “anello” che non possiede la corretta priorità d’intervento sono effettivamente tempo ed energie tolte all’“anello” più debole che impatta, in quel momento di vita specifico, maggiormente sull’accorciamento dei telomeri e quindi all’ aspettativa di vita della persona.
Nella metafora del modello a “catena” potremmo dire che l’obiettivo del professionista è quello di evitare che ci siano anelli “di carta” piuttosto che rinforzare uno o più anelli per farli diventare “di titanio”.
Nella logica della catena, infatti, che ci sia un anello, o più anelli, “di titanio” accoppiati ad uno o più anelli “di carta” rende comunque la catena stessa molto fragile.
Per la natura globale ed integrata della catena (“la catena è forte quanto il più debole dei suoi anelli”) la strategia migliore che ottimizza la sua resistenza è quella di rinforzare gli anelli più deboli fino a farli diventare resistenti quanto gli anelli più forti.
Chiaramente una catena composta da nove anelli di ferro è molto più resistente di una catena composta otto anelli di titanio ed uno di carta.
Le dinamiche caratteristiche del modello a “catena” sembrano anche riflettere in maniera più realistica la complessità e l’eterogeneità dei comportamenti e delle performance umane, infatti, risulta maggiormente esplicativo rispetto i modelli gerarchici che prevedono la dominanza di un fattore sugli altri.
Per esempio, i casi agli antipodi delle morti premature di sportivi professionisti che hanno condotto per molti anni intense attività motorie e che hanno seguito una corretta alimentazione ed i casi degli ultracentenari che pur non avendo mai fatto un’attività motoria particolarmente intensa (non essendo però mai stati sedentari) e malgrado un’alimentazione non ottimale (ma che non è mai stata scadente per lunghi periodi), rappresentano performance di longevità agli molto distanti che possono essere comprese unicamente dal modello a “catena” e non dai modelli gerarchici che prevedono invece ad esempio l’alimentazione e l’attività motoria come fattori dominanti più impattanti (rispetto altri fattori) sulla salute ed il benessere umano.
Il modello a “catena” appena descritto chiaramente rappresenta una sfida culturale rispetto l’attuale formazione iper-specialistica ed ultra-settoriale che da decenni è largamente condivisa sia a livello universitario che post-universitario le comunità professionali.
Gli attuali paradigmi iper-specialistici si declinano infatti in protocolli clinici utilizzati dai professionisti che di conseguenza, nel supportare i propri pazienti, tendono a sottostimare grandemente la dimensione integrata e globale delle persone.
Sebbene nell’ultimo secolo i progressi biomedici registrati nel trattare le problematiche acute e traumatiche siano evidenti e degni di ammirazione e gratitudine, l’altrettanto evidente bassa efficacia degli interventi nel gestire le attuali problematiche croniche riflette questo approccio riduzionistico, specialistico e gerarchico per alcuni aspetti opposto a quello qui descritto come modello a “catena”.
Se il modello a “catena” dovesse confermarsi prezioso dal punto di vista clinico sarebbe auspicabile che venisse integrato quanto prima nei percorsi formativi dei professionisti della salute e del benessere umano ma anche promosso e condiviso attraverso opportune comunicazioni rivolte ai cittadini.
Questo articolo e' la traduzione italiana della mia pubblicazione americana:
Agnoletti, M. (2025). A new integrated model of health derived from telomere science: the “chain” model, in book Complexity and Fractality in Human Change and Beyond, Nova Science Publishers, USA.
Agnoletti, M. (2019). L’Effetto Imbuto o Effetto Collo di Bottiglia dei telomeri, Medicalive Magazine, 5, 18-21.
Agnoletti, M. (2018a). L’Asse psiche-telomeri ecco come la mente influenza l’invecchiamento. PNEINEWS, 5, 4-8.
Agnoletti, M. (2018b). La Scienza dei Telomeri. Come sta cambiando radicalmente il concetto d’invecchiamento con importanti conseguenze sul piano della salute e del benessere psicofisico umano. Medicalive Magazine, 8, 5-7.
Agnoletti, M. (2018c). La nuova frontiera della psicologia: la Psicologia Epigenetica. State of Mind, 10. https://www.stateofmind.it/2018/10/psicologia-epigenetica/
Agnoletti, M. (2018d). La Scienza dei Telomeri e il modello integrato di salute psicofisica. Medicalive Magazine, 11, 8-10.
Agnoletti, M. (2021). L’olobionte umano-microbiota e l’effetto imbuto dei telomeri. State of Mind, 10. https://www.stateofmind.it/2021/10/olobionte-microbiota-telomeri/
Agnoletti, M. (2022). L’effetto imbuto dei telomeri sui protocolli di supporto psicofisico. State of Mind, 5. https://www.stateofmind.it/2022/05/telomeri-effetto-imbuto/
Al-Hazzouri, A. Z., Stone, K. L., Hough, C. M., Yaffe, K., & Stewart, A. L. (2014). Sleep duration and telomere length in a sample of older men: results from the Osteoporotic Fractures in Men Study. Journal of Aging Research, 2014, 819341.
Andrews, B. & Cornell, J. (2014). Telomere Basics: Curing Aging. Nevada, USASierra Science.
Andrews, B. & Cornell, J. (2017). Telomere Lenghtening. Nevada, USA. Sierra Science.
Armanios, M., & Blackburn, E. H. (2012). The telomere syndromes. Nature Reviews Genetics, 13(10), 693-704.
Aubert, G., & Lansdorp, P. M. (2008). Telomeres and aging. Physiological Reviews, 88(2), 557-579.
Blackburn, E. H., & Epel, E. S. (2015). Telomeres and adversity: Too toxic to ignore. Cell, 162(4), 709-711.
Blackburn, E. H., Epel, E. S., & Lin, J. (2015). Human telomere biology: A contributory and interactive factor in aging, disease risks, and protection. Science, 350(6265), 1193-1198.
Bojesen, S. E. (2013). Telomeres and human health. Journal of Internal Medicine, 274(5), 399-413.
Cacioppo, J. T., Hawkley, L. C., & Thisted, R. A. (2010). Perceived social isolation makes me sad: five year cross-lagged analyses of loneliness and depressive symptomatology in the Chicago Health, Aging, and Social Relations Study. Psychology and Aging, 25(2), 453-463.
Calado, R. T., & Young, N. S. (2009). Telomere diseases. New England Journal of Medicine, 361(24), 2353-2365.
Carroll, J. E., Esquivel, S., Goldberg, A., Seeman, T. E., Effros, R. B., Dock, J., ... & Olmstead, R. (2016). Insomnia and telomere length in older adults. Sleep, 39(3), 559-564.
Carroll, J. E., Seeman, T. E., Olmstead, R., Melendez, G., Sadakane, R., & Freedland, K. E. (2016). Improved sleep, psychological well-being, and circadian rhythms predict long-term improvements in telomere length in caregivers of patients with Alzheimer's disease. Sleep, 39(9), 1503-1511.
Cawthon, R. M., Smith, K. R., O'Brien, E., Sivatchenko, A., & Kerber, R. A. (2003). Association between telomere length in blood and mortality in people aged 60 years or older. The Lancet, 361(9355), 393-395.
Cherkas, L. F., Hunkin, J. L., Kato, B. S., Richards, J. B., Gardner, J. P., Surdulescu, G. L., ... & Aviv, A. (2008). The association between physical activity in leisure time and leukocyte telomere length. Archives of Internal Medicine, 168(2), 154-158. https://doi.org/10.1001/archinternmed.2007.39
Clemente, D. B. P., Vrijheid, M., Martens, D. S., Plusquin, M., Nawrot, T. S., & Janssen, B. G. (2020). Prenatal ambient air pollution, placental mitochondrial DNA content and telomere length: An ENVIRONAGE birth cohort study. Environment International, 138, 105597.
Crous-Bou, M., Fung, T. T., Prescott, J., Julin, B., Du, M., Sun, Q., ... & De Vivo, I. (2014). Mediterranean diet and telomere length in Nurses' Health Study: population based cohort study. BMJ, 349, g6674.
D'Mello, M. J., Ross, S. A., Briel, M., Anand, S. S., Gerstein, H., & Paré, G. (2015). Association between shortened leukocyte telomere length and cardiometabolic outcomes: Systematic review and meta-analysis. Circulation: Cardiovascular Genetics, 8(1), 82-90.
Dioni, L., Hoxha, M., Nordio, F., Tarantini, L., Albetti, B., Grillo, G., ... & Baccarelli, A. A. (2011). Effects of short-term exposure to inhalable particulate matter on telomere length, telomerase expression, and telomerase methylation in elderly adults. Environmental Health Perspectives, 119(5), 737-742.
Engel, G. L. (1977). The need for a new medical model. A challenge for biomedicine. Science. 196, 129-136.
Epel, E. S., & Prather, A. A. (2018). Stress, telomeres, and psychopathology: Toward a deeper understanding of a triad of early aging. Annual Review of Clinical Psychology, 14, 371-397.
Epel, E. S., Blackburn, E. H., Lin, J., Dhabhar, F. S., Adler, N. E., Morrow, J. D., & Cawthon, R. M. (2004). Accelerated telomere shortening in response to life stress. Proceedings of the National Academy of Sciences, 101(49), 17312-17315.
Epel, E. S., Puterman, E., Lin, J., Blackburn, E. H., Lum, P. Y., Beckmann, N. D., ... & Mangino, M. (2016). Meditation and vacation effects have an impact on disease-associated molecular phenotypes. Translational Psychiatry, 6(8), e880.
Fitzpatrick, A. L., Kronmal, R. A., Gardner, J. P., Psaty, B. M., Jenny, N. S., Tracy, R. P., ... & Aviv, A. (2007). "Leukocyte telomere length and cardiovascular disease in the Cardiovascular Health Study." American Journal of Epidemiology, 165(1), 14-21.
Garcia-Calzon, S., Moleres, A., Marcos, A., Campoy, C., Martinez-Gonzalez, M. A., Azcona-San Julian, M. C., ... & Marti, A. (2014). Telomere length as a biomarker for adiposity changes after a multidisciplinary intervention in adolescents: The EVASYON study. PLOS ONE, 9(2), e89828.
Ghosh, S., Sinha, J. K., Raghunath, M., & Chakrabarti, S. (2017). Increase in the gut microbiota diversity in short-lived ERCC1−/− mice fed with a probiotic mix correlates with improved health and lifespan: Prospects of microbe-based interventions to counteract aging. Ageing Research Reviews, 36, 62-74.
Gotlib, I. H., & LeMoult, J. (2019). Telomere length and early life stress: An overview of research and the need for integrated approaches. Journal of Behavioral Medicine, 42(4), 535-543.
Harley, C. B., Futcher, A. B., & Greider, C. W. (1990). Telomeres shorten during ageing of human fibroblasts. Nature, 345(6274), 458-460.
Hayflick, L., & Moorhead, P. S. (1961). "The serial cultivation of human diploid cell strains." Experimental Cell Research, 25(3), 585-621.
Hoxha, M., Dioni, L., Bonzini, M., Pesatori, A. C., Fustinoni, S., Cavallo, D., ... & Baccarelli, A. (2009). Association between leukocyte telomere shortening and exposure to traffic pollution: A cross-sectional study on traffic officers and indoor office workers. Environmental Health, 8, 41.
Jackowska, M., Hamer, M., Carvalho, L. A., & Steptoe, A. (2012). Short sleep duration is associated with shorter telomere length in healthy men: findings from the Whitehall II cohort study. PLOS ONE, 7(10), e47292.
Jiang, X., Zhong, W., Zhang, G., Zheng, Z., Lan, Z., & Xu, L. (2017). Association between gut microbiota and telomere length in colorectal cancer patients. Journal of Digestive Diseases, 18(12), 580-585.
Leung, C. W., Fung, T. T., McEvoy, C. T., Lin, J., Epel, E. S., & Dieterich, D. M. (2018). Associations of dietary intake and dietary patterns with leukocyte telomere length in a multi-ethnic sample of older adults: the Multi-Ethnic Study of Atherosclerosis (MESA). American Journal of Clinical Nutrition, 108(2), 165-175.
Li, J., Hand, G. A., & Wang, X. (2020). The impact of poor sleep on telomere length: A systematic review. Journal of Clinical Sleep Medicine, 16(6), 981-987.
Lin, J., Epel, E., & Blackburn, E. (2012). Telomeres and lifestyle factors: Roles in cellular aging. Mutation Research/Fundamental and Molecular Mechanisms of Mutagenesis, 730(1-2), 85-89.
Liu, T., Hougen, H. Y., Qi, X., & Yu, J. (2020). Associations between gut microbiota and telomere biology: New insights into the impact of diet and lifestyle. Nutrients, 12(6), 1868.
Liu, Y., & Khaing, A. A. (2012). Telomere dysfunction in human diseases: A review of recent progresses in experimental and clinical researches. Journal of Genetics and Genomics, 39(1), 9-22.
Liu, Y., Cao, H., Song, S., & Miao, Y. (2018). Multiple environmental and genetic factors act in an integrated manner to negatively regulate telomere length and protect telomere capping in Arabidopsis. Frontiers in Plant Science, 9, 1444.
Lynch, B. M., et al. (2020). Physical activity and telomere length in early stage breast cancer survivors. Breast Cancer Research, 22, 56. https://doi.org/10.1186/s13058-020-01298-0
Marcon, F., Siniscalchi, E., Crebelli, R., Veneziano, S., Pensa, A., & Sgura, A. (2012). Diet-related telomere shortening and chromosome stability. Mutagenesis, 27(1), 49-57.
McGrath, E. E., Jones, A., & Sorkin, J. D. (2017). Air pollution and telomere length: A systematic review of the literature. Journal of Public Health Research, 6(3), 1040.
Munstock, L., et al. (2021). Physical activity on telomere length as a biomarker for aging: A systematic review. Sports Medicine - Open, 7(1), 41. https://doi.org/10.1186/s40798-021-00315-3
Needham, B. L., Mezuk, B., Bareis, N., Lin, J., Blackburn, E. H., & Epel, E. S. (2015). Depression, anxiety and telomere length in young adults: evidence from the National Health and Nutrition Examination Survey. Molecular Psychiatry, 20(4), 520-528.
Niles, J. K., Joshi, A. D., & Terry, M. B. (2016). Diet, telomere length, and cancer risk: A review of potential mechanisms and epidemiological evidence. Cancer Causes & Control, 27(6), 845-858.
O'Donovan, A., Slavich, G. M., Epel, E. S., & Neylan, T. C. (2013). Exaggerated neurobiological sensitivity to threat as a mechanism linking anxiety with increased risk for diseases of aging. Neuroscience & Biobehavioral Reviews, 37(1), 96-108.
Prather, A. A., Puterman, E., Lin, J., O'Donovan, A., Krauss, J., Tomiyama, A. J., ... & Epel, E. S. (2011). Shorter leukocyte telomere length in midlife women with poor sleep quality. Journal of Aging Research, 2011, 721390.
Price, L. H., Kao, H. T., Burgers, D. E., Carpenter, L. L., & Tyrka, A. R. (2013). Telomeres and early-life stress: An overview. Biological Psychiatry, 73(1), 15-23.
Puterman, E., Epel, E. S., O'Donovan, A., Prather, A. A., Aschbacher, K., Dhabhar, F. S., ... & Blackburn, E. H. (2013). Predictors of telomere length in the Health and Retirement Study: New insights into resilient aging. Psychoneuroendocrinology, 38(9), 2418-2427.
Puterman, E., Lin, J., Blackburn, E., O’Donovan, A., Adler, N., & Epel, E. (2010). The power of exercise: buffering the effect of chronic stress on telomere length. PLoS ONE, 5(7), e10837. https://doi.org/10.1371/journal.pone.0010837
Ridout, K. K., Ridout, S. J., Price, L. H., Sen, S., & Tyrka, A. R. (2016). Depression and telomere length: A meta-analysis. Journal of Affective Disorders, 191, 237-247.
Savolainen, K., Eriksson, J. G., Kajantie, E., Lahti, J., Lahti, M., Heinonen, K., ... & Räikkönen, K. (2014). Telomere length and hypothalamic-pituitary-adrenal axis response to stress in elderly adults. Psychoneuroendocrinology, 47, 12-17.
Schwartz, G. E. (1982). Testing the biopsychosocial model: The ultimate challenge facing behavioral medicine? Journal of Consulting and Clinical Psychology, 50(6): 1040-1053.
Shalev, I., Entringer, S., Wadhwa, P. D., Wolkowitz, O. M., Puterman, E., Lin, J., ... & Epel, E. S. (2013). "Stress and telomere biology: A lifespan perspective." Psychoneuroendocrinology, 38(9), 1835-1842.
Shalev, I., Moffitt, T. E., Sugden, K., Williams, B., Houts, R. M., Danese, A., ... & Caspi, A. (2013). Exposure to violence during childhood is associated with telomere erosion from 5 to 10 years of age: A longitudinal study. Molecular Psychiatry, 18(5), 576-581.
Shammas, M. A. (2011). Telomeres, lifestyle, cancer, and aging. Current Opinion in Clinical Nutrition & Metabolic Care, 14(1), 28-34.
Simon, N. M., Smoller, J. W., McNamara, K. L., Maser, R. S., Zalta, A. K., Pollack, M. H., ... & Wong, K. K. (2006). Telomere shortening and mood disorders: preliminary support for a chronic stress model of accelerated aging. Biological Psychiatry, 60(5), 432-435.
Starr, J. M., Shiels, P. G., Harris, S. E., & Deary, I. J. (2008). Telomere length and lifetime cognitive change: Combined effect of early and later life adversity. Neurobiology of Aging, 29(2), 269-276.
Steptoe, A., Owen, N., Kunz-Ebrecht, S. R., & Brydon, L. (2004). Loneliness and neuroendocrine, cardiovascular, and inflammatory stress responses in middle-aged men and women. Psychoneuroendocrinology, 29(5), 593-611.
Tejada-Garrido, C. I., Martín-Vallejo, J., & Navarro-López, V. (2024). Effects of physical exercise on telomere length in healthy adults: Systematic review, meta-analysis, and meta-regression. JMIR Public Health and Surveillance, 10, e46019. https://doi.org/10.2196/46019
Tucker, L. A. (2017). Physical activity and telomere length in U.S. men and women: An NHANES investigation. Preventive Medicine, 100, 145-151.
Vaiserman, A. M., & Krasnienkov, D. S. (2021). Telomere length as a marker of biological aging: State-of-the-art, open issues, and future perspectives. Frontiers in Genetics, 11, 630186.
Valdes, A. M., Andrew, T., Gardner, J. P., Kimura, M., Oelsner, E., Cherkas, L. F., ... & Spector, T. D. (2005). Obesity, cigarette smoking, and telomere length in women. The Lancet, 366(9486), 662-664.
Ward-Caviness, C. K., Kraus, W. E., Blach, C., Haynes, C. S., Dowdy, E., Miranda, M. L., & Mukherjee, B. (2016). Association of roadside air pollution with cardiovascular disease biomarkers in commuters: A panel study. Environmental Research, 146, 116-124.
Wen, W., Luo, S., Zhang, S., & Liang, X. (2015). The influence of circadian rhythm on the length of telomeres and the mechanism of aging. Progress in Biophysics and Molecular Biology, 119(2), 128-135.
Zhang, J., Rane, G., Dai, X., Shanmugam, M. K., Arfuso, F., Samy, R. P., ... & Sethi, G. (2016). Ageing and the telomere connection: An intimate relationship with inflammation. Ageing Research Reviews, 25, 55-69.
Zhu, Y., Xiang, Q., Xie, S., Zheng, J., & Zhang, X. (2019). Interaction between circadian rhythm and depression on telomere length and metabolic parameters in women: a cross-sectional study. Journal of Affective Disorders, 256, 162-168.

 Mi chiamo Massimo Agnoletti, sono uno psicologo, un dottore di ricerca e uno specialista dello stress. Ho un'esperienza professionale internazionale, soprattutto negli USA, e da sempre ho la passione di studiare la psicologia scientifica per tradurla in modalità concrete ed applicabili al fine di migliorare il benessere delle persone.
Mi chiamo Massimo Agnoletti, sono uno psicologo, un dottore di ricerca e uno specialista dello stress. Ho un'esperienza professionale internazionale, soprattutto negli USA, e da sempre ho la passione di studiare la psicologia scientifica per tradurla in modalità concrete ed applicabili al fine di migliorare il benessere delle persone.